-
L'illustration ci-dessous correspond à la réaction chimique entre l'aluminium et le diiode.
Elle démarre quand on met une goutte d'eau sur le mélange des réactifs.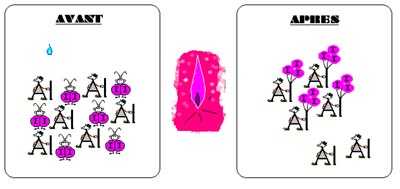
La réaction schématisée met elle en évidence un réactif limitant ?
Consulter, si nécessaire, Aidechim pour avoir des précisions sur ce qu'est un réactif limitant (glossaire). -
Quel est le réactif limitant ?
-
Regardez à nouveau attentivement l'illustration.

Quelle est l'équation-bilan qui correspond à cette illustration ? -
Pour répondre à cette question vous devez consulter la vidéo de la réaction correspondante.
La réaction chimique est ... -
Quelle est la quantité de matière d'aluminium présente initialement ?
Vous pouvez consulter le protocole expérimental de cette réaction. -
Quelle est la quantité de matière de diiode présente initialement ?
Vous avez oublié la masse de diiode utilisée ? N'hésitez pas à reconsulter le protocole expérimental ! -
Dans ces conditions, quelle est la composition du système en fin de réaction ?
Rappel : l'équation-bilan est :4 Al + 3 I2 = 2 Al2I3 -
La réaction décrite dans le protocole expérimental, se fait-elle avec un réactif limitant ? Si oui, quel est ce réactif ?
-
Quelle est la masse de triiodure d'aluminium obtenue (en supposant le rendement de la réaction de 100 %) ?
Indication : calculer, au préalable, la masse molaire du triodure d'aluminium.