Origine des macromolécules
du vivant
Robert PASCAL - robert.pascal@univ-montp2.fr
1) Institut des Biomolécules Max Mousseron UMR5247, CNRS - Universités
Montpellier 1 & 2 Place Eugène Bataillon, 34095 Montpellier
Cedex 5
 Résumé de
la présentation fourni par le conférencier : L'évolution
des êtres vivants utilise la variabilité liée
au choix de monomères particuliers pris dans un ensemble fini (acides
aminés, nucléotides) pour
constituer la séquence bien définie de macromolécules
(acides nucléiques ou protéines).
Ces macromolécules sont l'objet de la sélection
naturelle qui s'exerce sur les organismes qui les portent, soit directement,
par leurs
propriétés, soit indirectement, par
le résultat de leurs fonctions. La reproduction d'informations épigénétiques
(non-codées)
ne joue en apparence, tout au moins aujourd'hui, qu'un rôle relativement
limité. La question de la formation de ces polymères
se pose donc dès
l'origine de la vie si l'on considère que leur activité est
nécessaire pour assurer
l'émergence d'un être vivant, mais aussi pour assurer l'auto-entretien
des générations suivantes.
Il
est donc difficile de séparer d'une part les voies abiotiques initiales
de formation de ces macromolécules et
d'autre part le métabolisme
ultérieur assurant leur reproduction
au sein des premiers organismes vivants, qui ont très probablement
continué d'exploiter
des voies abiotiques disponibles dans l'environnement durant les premiers
stades de l'évolution. L'action de la sélection naturelle sur
les fonctions codées
présentes chez ces organismes n'exclut en aucune manière la
participation additionnelle d'autres espèces de petites tailles fournies
par l'environnement, qui s'intégreraient comme métabolites
ou catalyseurs pouvant constituer des cycles métaboliques (éventuellement
autocatalytiques). Des polymères aléatoires (petits peptides
par exemple) peuvent également
jouer un rôle. Toutes ces molécules peuvent être l'objet
d'une sélection,
mais à la différence des macromolécules de séquence
définies, leur rôle
ne peut être transmis de manière codée. Nous aborderons
les progrès faits ces dernières années
dans la compréhension des voies abiotiques de synthèse des
monomères, des voies proto-métaboliques
disponibles et de l'apport énergétique nécessaire à la
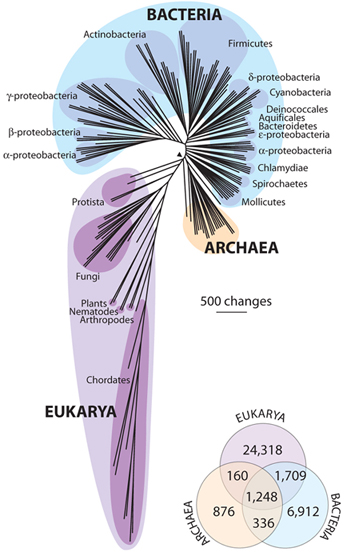
polymérisation. - Schéma :
Comparaison des génomes de 185 organismes et mise en évidence
des éléments
communs relativement aux protéines. La fléchette à l'intersection
des trois est la racine vers LUCA. -
Résumé de
la présentation fourni par le conférencier : L'évolution
des êtres vivants utilise la variabilité liée
au choix de monomères particuliers pris dans un ensemble fini (acides
aminés, nucléotides) pour
constituer la séquence bien définie de macromolécules
(acides nucléiques ou protéines).
Ces macromolécules sont l'objet de la sélection
naturelle qui s'exerce sur les organismes qui les portent, soit directement,
par leurs
propriétés, soit indirectement, par
le résultat de leurs fonctions. La reproduction d'informations épigénétiques
(non-codées)
ne joue en apparence, tout au moins aujourd'hui, qu'un rôle relativement
limité. La question de la formation de ces polymères
se pose donc dès
l'origine de la vie si l'on considère que leur activité est
nécessaire pour assurer
l'émergence d'un être vivant, mais aussi pour assurer l'auto-entretien
des générations suivantes.
Il
est donc difficile de séparer d'une part les voies abiotiques initiales
de formation de ces macromolécules et
d'autre part le métabolisme
ultérieur assurant leur reproduction
au sein des premiers organismes vivants, qui ont très probablement
continué d'exploiter
des voies abiotiques disponibles dans l'environnement durant les premiers
stades de l'évolution. L'action de la sélection naturelle sur
les fonctions codées
présentes chez ces organismes n'exclut en aucune manière la
participation additionnelle d'autres espèces de petites tailles fournies
par l'environnement, qui s'intégreraient comme métabolites
ou catalyseurs pouvant constituer des cycles métaboliques (éventuellement
autocatalytiques). Des polymères aléatoires (petits peptides
par exemple) peuvent également
jouer un rôle. Toutes ces molécules peuvent être l'objet
d'une sélection,
mais à la différence des macromolécules de séquence
définies, leur rôle
ne peut être transmis de manière codée. Nous aborderons
les progrès faits ces dernières années
dans la compréhension des voies abiotiques de synthèse des
monomères, des voies proto-métaboliques
disponibles et de l'apport énergétique nécessaire à la
polymérisation. - Schéma :
Comparaison des génomes de 185 organismes et mise en évidence
des éléments
communs relativement aux protéines. La fléchette à l'intersection
des trois est la racine vers LUCA. -
7/ Préambule : Ayant eu les plus grandes difficultés à comprendre l'exposé très technique de Robert Pascal durant le colloque, j'ai fait des recherches à partir du diaporama qu'il a présenté et des quelques notes que j'ai prises, et je présente ici une compilation de diverses sources, cours, diaporamas, articles, publiés sur Internet, dont le sujet se rapproche le plus de celui qui a été traité au colloque.
Sur la centaine d'atomes
que l'on trouve dans l'univers, 24 sont nécessaires aux êtres
vivants pour former des molécules de très grande taille
constituées
de l'enchaînement
de molécules plus petites, les monomères, et agencées
en une
structure de base unique, la cellule. Les trois branches du vivant,
archaea, bactéries
et eucaryotes,
ont des éléments en commun, il est donc impossible de
déterminer une chronologie d'apparition en arborescence comme
on l'imaginait
autrefois.
L'évolution a dû procéder en
'buisson' dont les trois branches maîtresses émaneraient
d'un tronc commun qui prendrait son origine en un ancêtre hypothétique,
 LUCA, "Last
Universal Common Ancestor" (le dernier ancêtre commun universel).
LUCA, "Last
Universal Common Ancestor" (le dernier ancêtre commun universel).
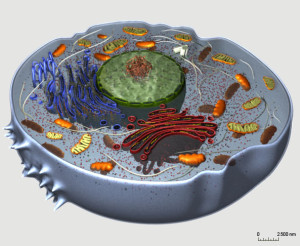
Toutefois, quel que soit ce LUCA, il est peu à peu devenu évident qu'il ne pouvait pas avoir été le premier être vivant sur Terre, car la réunion de ces caractéristiques communes formaient un organisme déjà très complexe. Il devait donc très certainement avoir été lui-même aussi le résultat d'une évolution préalable, le problème étant de savoir selon quel processus. Pour l'analyser, les scientifiques oeuvrent de deux manières différentes. D'une part, ils poursuivent l'étude de toutes les sortes de cellules existantes, et s'intéressent tout particulièrement à leurs composants, qui ont pu être des organismes primitifs intégrés plus tard dans ces organismes plus complexes. D'autre part, ils mettent en présence en laboratoire des matériaux qu'ils supposent avoir été disponibles dans les premiers temps de la Terre, en essayant de reconstituer l'environnement qui prévalait alors (température, composition de l'atmosphère et des océans, etc.). C'est cette seconde voie qu'a choisie Robert Pascal. - Schéma : Cellule animale. -
Il
cherche à comprendre les étapes qui ont permis à la
matière de passer
du non-vivant au vivant, ou plus exactement à la cellule (les
scientifiques considèrent
généralement
que les virus ne sont pas pleinement vivants, puisqu'ils n'ont pas de
capacité
de reproduction autonome). En préalable,
dans un exposé-bilan,
il définit le
vivant comme un ensemble confiné,
possédant
un contenu informationnel réplicable, doté d'un
métabolisme
et soumis à une évolution darwinienne, ce qui l'amène à
se poser la question suivante. 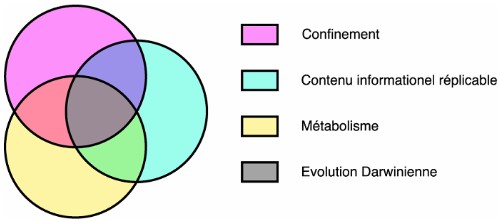 Qu'est-ce
qui est d'abord apparu, le métabolisme,
l'information génétique,
la membrane, ou bien y a-t-il eu une coévolution de ces
éléments ? L'alternative classique, 'Le métabolisme
d'abord !', 'Le porteur d'information génétique d'abord
!', lui semble une vision très réductrice. S'appuyant
sur les travaux d'Iris
Fry, il
prône l'idée d'un 'métabolisme préparatoire' à la
voie 'gène d'abord'.
Selon lui, il est difficile de séparer les premières
voies (métaboliques)
de reproduction des macromolécules de la formation initiale
des premières
d'entre elles. Par conséquent, il s'agit de déterminer
les processus chimiques les plus anciens, sachant que la Terre disposait
de molécules
biologiques déjà pré-assemblées, soit
en provenance de l'espace et transportées par
les micro-météorites, météorites et
comètes,
soit générées par son atmosphère, et,
accessoirement peut-être,
dans les fumeurs noirs au fond des mers et
dans les sources hydrothermales. La
seule certitude, c'est que les premières
traces de vie sur Terre remontent à la période 3,5
- 3 Ga (giga ou milliards d'années), et que celle-ci a fort
bien pu émerger
plus tôt,
entre 4,4 et 3,8 Ga.
Qu'est-ce
qui est d'abord apparu, le métabolisme,
l'information génétique,
la membrane, ou bien y a-t-il eu une coévolution de ces
éléments ? L'alternative classique, 'Le métabolisme
d'abord !', 'Le porteur d'information génétique d'abord
!', lui semble une vision très réductrice. S'appuyant
sur les travaux d'Iris
Fry, il
prône l'idée d'un 'métabolisme préparatoire' à la
voie 'gène d'abord'.
Selon lui, il est difficile de séparer les premières
voies (métaboliques)
de reproduction des macromolécules de la formation initiale
des premières
d'entre elles. Par conséquent, il s'agit de déterminer
les processus chimiques les plus anciens, sachant que la Terre disposait
de molécules
biologiques déjà pré-assemblées, soit
en provenance de l'espace et transportées par
les micro-météorites, météorites et
comètes,
soit générées par son atmosphère, et,
accessoirement peut-être,
dans les fumeurs noirs au fond des mers et
dans les sources hydrothermales. La
seule certitude, c'est que les premières
traces de vie sur Terre remontent à la période 3,5
- 3 Ga (giga ou milliards d'années), et que celle-ci a fort
bien pu émerger
plus tôt,
entre 4,4 et 3,8 Ga.
 Les
processus qui se déroulent
dans les cellules sont très élaborés et
certains scientifiques se demandent s'il n'y a pas pu avoir un stade
préliminaire
où l'ADN (acide
désoxyribonucléique),
porteur de l'information génétique, n'existait pas encore.
En effet, celui-ci,
dont on connaît la structure depuis 1953, est formé d'un enchaînement
de 4 nucléotides désignés chacun en abrégé par
l’une des 4 lettres désignant leurs composants appelés « bases » :
A, T, G ou C (adénine, thymine, guanine, cytosine). Leur enchaînement,
comme s’il
s’agissait d’un alphabet, peut générer
de très nombreuses combinaisons, plus ou moins longues et complexes
: cette façon de coder l’information à transmettre
est la première caractéristique de l’ADN.
Les
processus qui se déroulent
dans les cellules sont très élaborés et
certains scientifiques se demandent s'il n'y a pas pu avoir un stade
préliminaire
où l'ADN (acide
désoxyribonucléique),
porteur de l'information génétique, n'existait pas encore.
En effet, celui-ci,
dont on connaît la structure depuis 1953, est formé d'un enchaînement
de 4 nucléotides désignés chacun en abrégé par
l’une des 4 lettres désignant leurs composants appelés « bases » :
A, T, G ou C (adénine, thymine, guanine, cytosine). Leur enchaînement,
comme s’il
s’agissait d’un alphabet, peut générer
de très nombreuses combinaisons, plus ou moins longues et complexes
: cette façon de coder l’information à transmettre
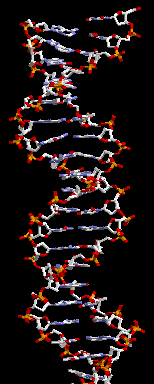
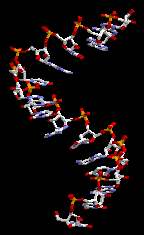
est la première caractéristique de l’ADN. C'est
une molécule
en forme de double hélice qui lui permet de se dupliquer à l’identique
lors de la division des cellules, et donc d’assurer la pérennité de
l’information, ce qui est sa deuxième caractéristique. -
Schéma : ADN. -
Une partie de notre ADN constitue les gènes au sein desquels les combinaisons des 4 lettres correspondent au codage d’une information génétique, nécessaire, après traduction dans les cellules, à la production de l’ensemble des protéines, enzymes, hormones, récepteurs etc. qui constituent notre corps. C’est l’organisation chromosomique, notamment l’ordre des gènes, qui est spécifique d’une espèce. L’ADN d'une cellule humaine pèse 7 millionièmes de millionième de gramme (picogramme), chaque brin est constitué de 3 milliards de paires de bases, recouvre 1 m si l’on déroule la molécule, et plus de 90 % de l’ADN est non codant et ne correspond donc pas aux gènes eux-mêmes qui sont au nombre de 50 000 environ (soit "seulement" 300 millions de paires de bases !). - Schéma : Protéine : assemblage d’un ou plusieurs polypeptides ayant subi des modifications post-traductionnelles et un repliement protéinique. Peptide : polymère d’acides aminés reliés entre eux par des liaisons peptidiques. Polypeptide : polymère comprenant un grand nombre d’acides aminés. -
L'ADN est donc le support de nos gènes et contient les instructions de production des protéines qui ont des fonctions de catalyse et de reconnaissance. Leur activité est liée à leur structure 3D (en 3 dimensions, conséquence d'une séquence déterminée et de son repliement) ; elle nécessite un système de traduction et l'homochiralité (pour qu'il y ait un ajustement possible de type clé/serrure). La réplication de l'ADN est assurée par des protéines, les ADN polymérases. Il en résulte un paradoxe 'de l'œuf et de la poule' si on se pose la question de savoir qui, des protéines ou de l'ADN, est apparu le premier au cours de l'émergence de la vie telle que nous la connaissons aujourd'hui. La difficulté provient du fait que ce ne sont pas les mêmes polymères qui portent l'information génétique (ADN) et les fonctions catalytiques nécessaires à la réplication (protéines). Ces deux sortes de polymères étant très complexes et chimiquement très différents, il était difficile d'imaginer comment ils avaient pu apparaître simultanément et indépendamment.
 Ces
chercheurs font alors l'hypothèse d'un Monde
d'ARN (acide ribonucléique), très proche chimiquement de
l'ADN dont il est généralement une copie partielle sur un
simple brin qui remplit diverses fonctions dans la cellule. Dans
les années 1980, Tom Cech et Sidney Altman découvrent
indépendamment que certains ARN, ensuite appelés ribozymes (contraction
de acide ribonucléique et enzymes), peuvent avoir un
rôle de catalyseur, comme les protéines.
Cette découverte inattendue leur vaut le prix
Nobel de chimie en 1989. Les ribozymes étant capables d'assurer à la
fois le rôle
de support de l'information génétique et de catalyseur, cela
permet de s'affranchir du paradoxe, en proposant que l'ARN soit le précurseur
unique, ce qui a été proposé en 1986 par Walter Gilbert,
le co-inventeur du séquençage de
l'ADN. Toutefois l'idée
d'une vie à base d'ARN est plus ancienne et remonte à Carl
Woese
dans 'The Genetic Code' (1967). Il est aussi
le découvreur des archaea comme troisième branche de l'évolution
et il va encore plus loin qu'un Monde d'ARN puisqu'il conteste l'idée
darwinienne d'un ancêtre unique pour toutes les formes de vie. Il pense
au contraire qu'un réseau d'êtres vivants a fréquemment
procédé à des échanges
d'ADN, ce qui signifierait qu'il y aurait plutôt de nombreuses 'racines' à l'origine
du vivant. - Schémas :
ARN. -
Ces
chercheurs font alors l'hypothèse d'un Monde
d'ARN (acide ribonucléique), très proche chimiquement de
l'ADN dont il est généralement une copie partielle sur un
simple brin qui remplit diverses fonctions dans la cellule. Dans
les années 1980, Tom Cech et Sidney Altman découvrent
indépendamment que certains ARN, ensuite appelés ribozymes (contraction
de acide ribonucléique et enzymes), peuvent avoir un
rôle de catalyseur, comme les protéines.
Cette découverte inattendue leur vaut le prix
Nobel de chimie en 1989. Les ribozymes étant capables d'assurer à la
fois le rôle
de support de l'information génétique et de catalyseur, cela
permet de s'affranchir du paradoxe, en proposant que l'ARN soit le précurseur
unique, ce qui a été proposé en 1986 par Walter Gilbert,
le co-inventeur du séquençage de
l'ADN. Toutefois l'idée
d'une vie à base d'ARN est plus ancienne et remonte à Carl
Woese
dans 'The Genetic Code' (1967). Il est aussi
le découvreur des archaea comme troisième branche de l'évolution
et il va encore plus loin qu'un Monde d'ARN puisqu'il conteste l'idée
darwinienne d'un ancêtre unique pour toutes les formes de vie. Il pense
au contraire qu'un réseau d'êtres vivants a fréquemment
procédé à des échanges
d'ADN, ce qui signifierait qu'il y aurait plutôt de nombreuses 'racines' à l'origine
du vivant. - Schémas :
ARN. -
Certains
scientifiques (comme le virologiste Patrick Forterre de l'institut de
génétique et microbiologie, à Orsay)
pensent que ce sont les virus qui seraient les "inventeurs" de
l'ADN.  L'apparition
de l'ADN viral dans un monde d'ARN serait une
solution de ces parasites pour déjouer les défenses cellulaires.
L'ADN présente plusieurs avantages évolutifs par rapport à l'ARN,
notamment une plus grande stabilité et la possibilité de détecter
les désaminations (génératrices de mutations) de C (cytosine)
en U (uracile), U n'étant pas normalement présent dans l'ADN,
mais seulement dans l'ARN. Toutefois, l'ARN est une molécule complexe
et fragile. Pour que l'hypothèse
du "Monde
d'ARN" soit crédible, il faut imaginer qu'un précurseur
ARN suffisamment long, capable de se répliquer, ait pu émerger
spontanément dans la soupe prébiotique. Cet événement
semble très improbable à un certain nombre de scientifiques.
Pour contourner cette difficulté, il a été proposé qu'un
précurseur plus simple que l'ARN ait précédé celui-ci.
Des phénomènes aussi fondamentaux et anciens sont très
difficiles à étayer, la longue évolution ayant effacé en
grande partie leurs éventuelles traces. -
Photo : Virus. -
L'apparition
de l'ADN viral dans un monde d'ARN serait une
solution de ces parasites pour déjouer les défenses cellulaires.
L'ADN présente plusieurs avantages évolutifs par rapport à l'ARN,
notamment une plus grande stabilité et la possibilité de détecter
les désaminations (génératrices de mutations) de C (cytosine)
en U (uracile), U n'étant pas normalement présent dans l'ADN,
mais seulement dans l'ARN. Toutefois, l'ARN est une molécule complexe
et fragile. Pour que l'hypothèse
du "Monde
d'ARN" soit crédible, il faut imaginer qu'un précurseur
ARN suffisamment long, capable de se répliquer, ait pu émerger
spontanément dans la soupe prébiotique. Cet événement
semble très improbable à un certain nombre de scientifiques.
Pour contourner cette difficulté, il a été proposé qu'un
précurseur plus simple que l'ARN ait précédé celui-ci.
Des phénomènes aussi fondamentaux et anciens sont très
difficiles à étayer, la longue évolution ayant effacé en
grande partie leurs éventuelles traces. -
Photo : Virus. -
Il a été également émis comme hypothèse l’émergence et le développement de la vie dans des milieux glacés, l’ARN se développant plus facilement dans la glace que dans des températures élevées (les nucléotides s’assemblent naturellement pour former des brins d’ARN lorsqu’ils sont dans un environnement gelé). A ce propos, de nouvelles recherches sur la météorite de Murchison tombée en Australie en 1969 ont révélé qu'elle abriterait des millions de molécules organiques différentes. En 2010, plus de 14 000 molécules organiques différentes ont été détectées, impliquant les 6 éléments principaux associés à la Vie, C, H, O, N, S et P (carbone, hydrogène, oxygène, azote, soufre, phosphore). Elle contient notamment des purines (les bases A, G de l'ADN appartiennent à cette catégorie de molécules), des pyrimidines (les bases T, C de l'ADN appartiennent à cette catégorie de molécules) et plus de 70 acides aminés, dont certains n’existent pas dans le monde vivant sur Terre.
 Qu’elle
soit intégrée
ou non à l’hypothèse d’un monde d’ARN,
la synthèse d’un porteur d’information semble à ce
jour une condition indispensable à l’émergence d’êtres
vivants. Pour que le résultat de la sélection naturelle
soit transmis aux générations suivantes, il est en effet
indispensable que l’information sélectionnée puisse être
répliquée. La synthèse d’un brin complémentaire à la
séquence initiale d’un acide nucléique puis sa recopie
sont les étapes déterminantes du processus. Le problème
est de trouver le métabolisme
préparatoire qui a permis la continuité évolutive
entre chimie prébiotique et évolution précoce. L'origine
de la vie date de l'émergence d'un polymère génétique à partir
d'un réseau de réactions chimiques (protométabolisme)
reposant sur l'activité de petites molécules ou de molécules
ne portant pas d'information. Ce protométabolisme est considéré
comme une "niche écologique" favorable
au développement d'un réplicateur génétique.
Si l'on s'intéresse à la transition, toute description
d'un mode de formation des peptides/acides nucléiques doit inclure
un métabolisme de ces composés sans faire la distinction
entre les deux stades de formation des monomères et d'activation/polymérisation.
Toutefois, si l'obtention d'acides aminés selon une voie abiotique
semble aisée
(1953, expérience de Miller), celle de nucléotides est
plus problématique.
L'ARN paraît indispensable, mais il est très difficile à synthétiser
dans un contexte prébiotique : il nécessite une formation
abiotique
de nucléotides, suivie de leur polymérisation. - Schéma :
Réplication de l'ADN. -
Qu’elle
soit intégrée
ou non à l’hypothèse d’un monde d’ARN,
la synthèse d’un porteur d’information semble à ce
jour une condition indispensable à l’émergence d’êtres
vivants. Pour que le résultat de la sélection naturelle
soit transmis aux générations suivantes, il est en effet
indispensable que l’information sélectionnée puisse être
répliquée. La synthèse d’un brin complémentaire à la
séquence initiale d’un acide nucléique puis sa recopie
sont les étapes déterminantes du processus. Le problème
est de trouver le métabolisme
préparatoire qui a permis la continuité évolutive
entre chimie prébiotique et évolution précoce. L'origine
de la vie date de l'émergence d'un polymère génétique à partir
d'un réseau de réactions chimiques (protométabolisme)
reposant sur l'activité de petites molécules ou de molécules
ne portant pas d'information. Ce protométabolisme est considéré
comme une "niche écologique" favorable
au développement d'un réplicateur génétique.
Si l'on s'intéresse à la transition, toute description
d'un mode de formation des peptides/acides nucléiques doit inclure
un métabolisme de ces composés sans faire la distinction
entre les deux stades de formation des monomères et d'activation/polymérisation.
Toutefois, si l'obtention d'acides aminés selon une voie abiotique
semble aisée
(1953, expérience de Miller), celle de nucléotides est
plus problématique.
L'ARN paraît indispensable, mais il est très difficile à synthétiser
dans un contexte prébiotique : il nécessite une formation
abiotique
de nucléotides, suivie de leur polymérisation. - Schéma :
Réplication de l'ADN. -
 Robert
Pascal fait part d'une découverte réalisée
par John Sutherland et son groupe de Manchester qui démontrent
que la formation de ribonucléotides
activés (des briques de base de l’ARN) est possible à partir
d’espèces très simples probablement présentes
dans un monde prébiotique. Mais la
voie utilisée est loin d’être
une reproduction de la voie biochimique actuelle, les composants du nucléotide
(base azotée, ribose, phosphate) ne sont pas des intermédiaires
de la synthèse qui se déroule par un chemin totalement différent.
L’avantage, c’est de court-circuiter le ribose, trop instable,
et de rendre inutile la condensation base-sucre, trop difficile. Il
est par ailleurs intéressant de noter que les phosphates jouent
des rôles
multiples dans cette voie de synthèse et pas seulement celui de
pont entre les briques de base. En résumé, au lieu d’essayer
de coupler sucre et base, ce que les chimistes n’ont pas réussi à faire
en 50 ans d’efforts, l’idée ici est de partir des précurseurs
des sucres et des bases, glycolaldéhyde, cyanamide, cyanoacétylène
pour obtenir en présence de phosphate un nucléotide activé.
Une
irradiation avec des UV permet de plus de dégrader les sous-produits
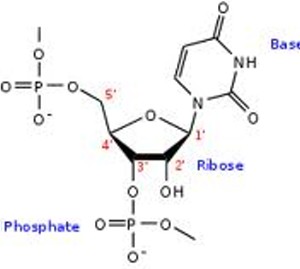
indésirables. - Schéma : Structure d'un
brin d'ARN. Les atomes du ribose sont numérotés. La base représentée
est l'uracile, qui n'est présente naturellement que dans l'ARN, à la
place de la thymine, présente dans l'ADN. -
Robert
Pascal fait part d'une découverte réalisée
par John Sutherland et son groupe de Manchester qui démontrent
que la formation de ribonucléotides
activés (des briques de base de l’ARN) est possible à partir
d’espèces très simples probablement présentes
dans un monde prébiotique. Mais la
voie utilisée est loin d’être
une reproduction de la voie biochimique actuelle, les composants du nucléotide
(base azotée, ribose, phosphate) ne sont pas des intermédiaires
de la synthèse qui se déroule par un chemin totalement différent.
L’avantage, c’est de court-circuiter le ribose, trop instable,
et de rendre inutile la condensation base-sucre, trop difficile. Il
est par ailleurs intéressant de noter que les phosphates jouent
des rôles
multiples dans cette voie de synthèse et pas seulement celui de
pont entre les briques de base. En résumé, au lieu d’essayer
de coupler sucre et base, ce que les chimistes n’ont pas réussi à faire
en 50 ans d’efforts, l’idée ici est de partir des précurseurs
des sucres et des bases, glycolaldéhyde, cyanamide, cyanoacétylène
pour obtenir en présence de phosphate un nucléotide activé.
Une
irradiation avec des UV permet de plus de dégrader les sous-produits
indésirables. - Schéma : Structure d'un
brin d'ARN. Les atomes du ribose sont numérotés. La base représentée
est l'uracile, qui n'est présente naturellement que dans l'ARN, à la
place de la thymine, présente dans l'ADN. -
 Il
reste ensuite à comprendre comment peut s'effectuer
une polymérisation spontanée de l'ARN. Un moyen d'y parvenir
a été imaginé par Nicholas Hud et
son équipe : en intercalant une molécule, le polymère
en cours de synthèse
n'a plus tendance à se replier en forme d'anneau, la
structure rendue ainsi plus rigide peut s'allonger par l'intégration
d'un grand nombre d'oligonucléotides. Le chercheur émet
l'hypothèse
que c'est cet intermédiaire (encore inconnu à ce jour) qui a permis
la sélection
des paires de bases contenues dans les acides nucléiques du vivant,
parmi toutes les molécules possibles. -
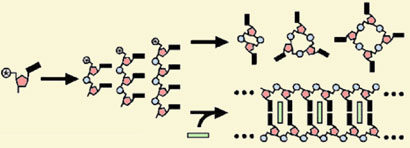
Schéma :
En présence d'une molécule intercalaire (verte), l'oligonucléotide
forme une longue chaîne de polymère, au lieu de s'arrêter à de
petites molécules
fermées (cyclisation).
-
Il
reste ensuite à comprendre comment peut s'effectuer
une polymérisation spontanée de l'ARN. Un moyen d'y parvenir
a été imaginé par Nicholas Hud et
son équipe : en intercalant une molécule, le polymère
en cours de synthèse
n'a plus tendance à se replier en forme d'anneau, la
structure rendue ainsi plus rigide peut s'allonger par l'intégration
d'un grand nombre d'oligonucléotides. Le chercheur émet
l'hypothèse
que c'est cet intermédiaire (encore inconnu à ce jour) qui a permis
la sélection
des paires de bases contenues dans les acides nucléiques du vivant,
parmi toutes les molécules possibles. -
Schéma :
En présence d'une molécule intercalaire (verte), l'oligonucléotide
forme une longue chaîne de polymère, au lieu de s'arrêter à de
petites molécules
fermées (cyclisation).
-
 Parallèlement,
Uwe Meierhenrich estime que la membrane qui
enclôt la cellule a un rôle primordial car elle permet le développement
contrôlé et la protection des réactions biologiques
dans son enceinte. Ce chercheur se dédie à l'étude
de la formation spontanée de vésicules «protocellulaires» à partir
de molécules amphiphiles (qui
possèdent à la
fois un groupe hydrophile et un groupe hydrophobe), à la
croissance et la division de ces vésicules primitives, à la
dynamique des membranes permettant l’absorption des nutriments et pouvant
conduire consécutivement à une élongation
de chaîne de dérivés nucléotidiques. En
ce qui concerne l'émergence de ce confinement,
Robert Pascal souligne qu'il a fallu que les composants du
système
s'associent
Parallèlement,
Uwe Meierhenrich estime que la membrane qui
enclôt la cellule a un rôle primordial car elle permet le développement
contrôlé et la protection des réactions biologiques
dans son enceinte. Ce chercheur se dédie à l'étude
de la formation spontanée de vésicules «protocellulaires» à partir
de molécules amphiphiles (qui
possèdent à la
fois un groupe hydrophile et un groupe hydrophobe), à la
croissance et la division de ces vésicules primitives, à la
dynamique des membranes permettant l’absorption des nutriments et pouvant
conduire consécutivement à une élongation
de chaîne de dérivés nucléotidiques. En
ce qui concerne l'émergence de ce confinement,
Robert Pascal souligne qu'il a fallu que les composants du
système
s'associent 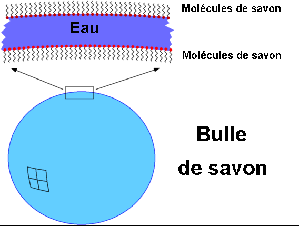 et
qu'un lien se constitue entre phénotype (ensemble
des caractères observables d'un individu, par exemple
la couleur des yeux) et
génotype (ensemble des informations génétiques
d'un individu). Il
s'interroge sur la formation des lipides (matière grasse
du vivant) qui constituent ces membranes cellulaires et sont
principalement
composés de
carbone, d’hydrogène et d’oxygène.
A-t-elle eu lieu selon une réaction
de type Fischer-Tropsch (*)
ou bien grâce à la constitution de membranes minérales
(**) ou encore au moyen d'un métabolisme
de surface(***) ? Un aspect essentiel du vivant est
qu'il transforme son environnement — c'est ce qu'on
appelle un métabolisme, c'est-à-dire l'incorporation, la
transformation et l'utilisation de certains produits de l'environnement.
C'est aussi un processus de synthèse et de recyclage des composants
de l'organisme qui assure l'auto-entretien. - Photo et schéma :
Exemple de molécules amphiphiles, la bulle de savon. -
et
qu'un lien se constitue entre phénotype (ensemble
des caractères observables d'un individu, par exemple
la couleur des yeux) et
génotype (ensemble des informations génétiques
d'un individu). Il
s'interroge sur la formation des lipides (matière grasse
du vivant) qui constituent ces membranes cellulaires et sont
principalement
composés de
carbone, d’hydrogène et d’oxygène.
A-t-elle eu lieu selon une réaction
de type Fischer-Tropsch (*)
ou bien grâce à la constitution de membranes minérales
(**) ou encore au moyen d'un métabolisme
de surface(***) ? Un aspect essentiel du vivant est
qu'il transforme son environnement — c'est ce qu'on
appelle un métabolisme, c'est-à-dire l'incorporation, la
transformation et l'utilisation de certains produits de l'environnement.
C'est aussi un processus de synthèse et de recyclage des composants
de l'organisme qui assure l'auto-entretien. - Photo et schéma :
Exemple de molécules amphiphiles, la bulle de savon. -
(*) A partir du charbon, du gaz ou de la biomasse, le procédé chimique industriel Fischer-Tropsch permet la synthèse d'hydrocarbures par la réaction du monoxyde de carbone avec de l'hydrogène grâce à l'effet catalytique du fer, du cobalt, du ruthénium ou du nickel, avec corrélativement un très fort rejet de gaz carbonique CO2 et donc un 'bilan carbone' très défavorable.
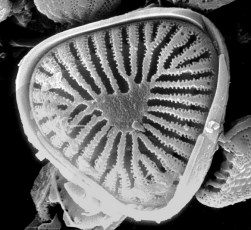 (**)
Exemple des diatomées.
Ce sont des algues brunes
qui stockent la silice. Son incorporation
se fait sous la forme d'acide monosilicique à travers la membrane à l'aide
de la pompe
Na-K (sodium-potassium). La silice se localise
d'abord dans une toute petite vésicule
au centre de la cellule puis va s'étendre dans le sens de la
longueur suivant une voie tracée par une membrane, la silicalemme.
Une première
couche de matériel dense se dépose. Quand elle atteint
une extrémité de la cellule elle revient vers le centre
en formant un U,
même chose pour l'autre moitié de la cellule simultanément
; enfin la silicalemme va fournir la trame de remplissage pour les
futurs dépôts de silice de la cellule qui se fait le long
des parois. - Photo : Diatomée lacustre du Miocène moyen
de Hellin en Espagne, observée au microscope électronique à balayage à un
grossissement de 4800 fois.
Cette diatomée mesure environ 16 µm.
Photo S. Servant, IRD. -
(**)
Exemple des diatomées.
Ce sont des algues brunes
qui stockent la silice. Son incorporation
se fait sous la forme d'acide monosilicique à travers la membrane à l'aide
de la pompe
Na-K (sodium-potassium). La silice se localise
d'abord dans une toute petite vésicule
au centre de la cellule puis va s'étendre dans le sens de la
longueur suivant une voie tracée par une membrane, la silicalemme.
Une première
couche de matériel dense se dépose. Quand elle atteint
une extrémité de la cellule elle revient vers le centre
en formant un U,
même chose pour l'autre moitié de la cellule simultanément
; enfin la silicalemme va fournir la trame de remplissage pour les
futurs dépôts de silice de la cellule qui se fait le long
des parois. - Photo : Diatomée lacustre du Miocène moyen
de Hellin en Espagne, observée au microscope électronique à balayage à un
grossissement de 4800 fois.
Cette diatomée mesure environ 16 µm.
Photo S. Servant, IRD. -
(***) Le métabolisme de surface (entretien sur France Culture avec Antoine Danchin). On a eu depuis longtemps l'idée que les êtres vivants sont nés dans une petite mare tiède (Darwin) et qu'il s'agissait pour eux de transformer des petites molécules au squelette carboné. Beaucoup se sont attachés à découvrir ces molécules dans l'environnement et ont cherché à démontrer l'existence de la vie et des possibilités d'un premier métabolisme à partir de ces molécules. Il semble en fait que l'idée d'une soupe, ce mélange dans lequel la vie serait née, est une idée inappropriée et que ce que l'on doit rechercher dans le métabolisme aujourd'hui est lié à une sélection de métabolites particuliers. Il faut donc trouver un processus capable de trier, parmi les différentes molécules organiques qui peuvent exister sur Terre, celles dont l'enchaînement va fonder la vie. De nos jours, les membranes jouent en partie ce rôle et c'est pour cette raison qu'elles sont si importantes dans la définition de l'individualité biologique ; mais on peut imaginer qu'initialement, le tri se soit fait surtout par les surfaces des pierres et des poussières : les molécules qui sont à l'origine du métabolisme auraient été triées par leurs charges électriques, en particulier par leurs charges négatives, qui leur permettaient de s'associer aux surfaces les plus courantes de la croûte terrestre. Si l'on se pose la question de l'origine en ces termes, on est ramené à un problème qui est très différent de celui de la soupe prébiotique puisqu'il s'agit de regarder ce qui se passe à la surface de solides, et non en solution.
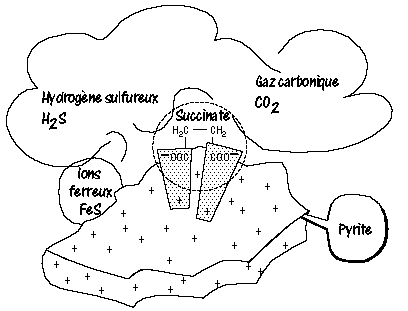 Or,
ce qui se passe en surface est extrêmement différent de ce
qui se passe en solution ; en particulier, les propriétés
de désagrégation
des gros édifices moléculaires, très importantes
en solution, disparaissent en surface et, dans ce cas, c'est non pas
la désagrégation
mais la polymérisation qui se trouve favorisée. L' idée
de base est donc de rechercher s'il existe aujourd'hui des traces de
ce qui aurait pu être initialement un métabolisme de surface
utilisant des molécules chargées. Gunther Wächtershaüser
s'est attaché à regarder
ce qui, dans la partie constructive du métabolisme actuel, est créateur
de formes vivantes. Il s'est rendu compte que cette partie constructive
appelée anabolisme
est constituée essentiellement de molécules soit porteuses
d'un groupe phosphate, soit porteuses de groupes carboxylates. Ce sont
dans les
deux cas des groupes chargés négativement dont on pourrait
penser qu'ils servent de pattes pour s’attacher à des surfaces
solides. Cette observation est très frappante, car lorsqu'on regarde
les transformations métaboliques et la chimie organique qui s'y
rattache, on se rend compte qu'aucun chimiste organicien ne procèderait
de la manière (apparemment
farfelue !) dont les choses se passent dans une cellule vivante. Au contraire,
on s'aperçoit
que ces molécules
sont parfaitement bien constituées pour fonctionner et
réagir
les unes avec les autres à la surface d'un solide. -
Schéma : Métabolisme de surface selon Gunther Wächtershaüser.
-
Or,
ce qui se passe en surface est extrêmement différent de ce
qui se passe en solution ; en particulier, les propriétés
de désagrégation
des gros édifices moléculaires, très importantes
en solution, disparaissent en surface et, dans ce cas, c'est non pas
la désagrégation
mais la polymérisation qui se trouve favorisée. L' idée
de base est donc de rechercher s'il existe aujourd'hui des traces de
ce qui aurait pu être initialement un métabolisme de surface
utilisant des molécules chargées. Gunther Wächtershaüser
s'est attaché à regarder
ce qui, dans la partie constructive du métabolisme actuel, est créateur
de formes vivantes. Il s'est rendu compte que cette partie constructive
appelée anabolisme
est constituée essentiellement de molécules soit porteuses
d'un groupe phosphate, soit porteuses de groupes carboxylates. Ce sont
dans les
deux cas des groupes chargés négativement dont on pourrait
penser qu'ils servent de pattes pour s’attacher à des surfaces
solides. Cette observation est très frappante, car lorsqu'on regarde
les transformations métaboliques et la chimie organique qui s'y
rattache, on se rend compte qu'aucun chimiste organicien ne procèderait
de la manière (apparemment
farfelue !) dont les choses se passent dans une cellule vivante. Au contraire,
on s'aperçoit
que ces molécules
sont parfaitement bien constituées pour fonctionner et
réagir
les unes avec les autres à la surface d'un solide. -
Schéma : Métabolisme de surface selon Gunther Wächtershaüser.
-
La question qui se pose alors est évidemment la création de la deuxième structure mentionnée tout au début, à savoir la membrane. La création d'une membrane est ce qui permet le passage en solution en empêchant la dilution à l'infini dans le milieu. Il est donc essentiel de regarder si, dans le métabolisme actuel, on peut imaginer un métabolisme de surface qui ait produit des molécules créant des membranes. Or, on observe quelque chose de très remarquable, c'est que la formation des lipides, qui sont des constituants essentiels des membranes, se fait à partir de précurseurs phosphorylés, ce qui est tout à fait étrange en dehors de l'hypothèse d'un métabolisme de surface. La polymérisation de ces molécules phosphorylées permettant la fabrication de lipides, on peut tout à fait imaginer qu'un métabolisme de surface ait produit des lipides, créant ainsi, autour des petites particules sur lesquelles ce métabolisme de surface est apparu, une membrane qui effectuera la sélection entre l'intérieur et l'extérieur et donc autorisera le passage en solution du métabolisme. Mais il faudra ensuite qu'intervienne un nouveau processus, tout à fait essentiel, à l'issue duquel la surface solide modifiée formera une matrice susceptible de passer en milieu liquide : il s'agit de trouver le substitut de la matrice solide.
 Or,
on a de véritables raisons
de penser que ce sont des acides ribonucléiques, des ARN,
qui ont été les
substituts des surfaces, car ces molécules sont justement
un peu comme les surfaces argileuses, par exemple, des polyanions
qui
attirent à leur
surface des charges positives, et peuvent ainsi servir de supports à d'autres
charges négatives ; ce sont donc éventuellement des
intermédiaires
obligés.
Or, parmi ces molécules il y a une classe, celle des ARN de
transfert, qui est justement au cœur du passage du programme
génétique à son
expression, et ces molécules sont très impliquées
dans le métabolisme actuel ; elles sont d'ailleurs fortement
affectées
par de petites modifications semblables à celles qui se déroulent
dans le métabolisme intermédiaire, et on les découvre
aujourd'hui dans un grand nombre de réactions qui n'ont rien à voir
avec la réaction de fabrication des protéines qui est
leur lieu normal de fonctionnement. On peut les trouver, par exemple,
associées à la
fabrication de liens peptidiques (entre acides aminés — le
cœur
de la synthèse des protéines), et l'on peut donc très
bien les imaginer comme étant des ancêtres de cette
réaction,
auquel cas la formation de liens peptidiques à partir de molécules
comme les ARN de transfert aurait été antérieure à l'utilisation
de cette formation de liens peptidiques dans la synthèse des
protéines
comme on la connaît aujourd'hui. Voici donc des objets bien
réels
qui ont pu jouer ce rôle de support métabolique, ce
qu'on peut essayer de mettre en évidence dans un certain nombre
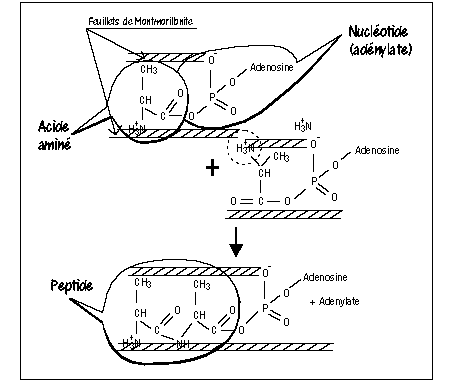
d'organismes. - Schéma : Formation d'une liaison peptidique
entre deux amino-acides adénylates pris "en sandwich" entre
deux feuillets d'argile. -
Or,
on a de véritables raisons
de penser que ce sont des acides ribonucléiques, des ARN,
qui ont été les
substituts des surfaces, car ces molécules sont justement
un peu comme les surfaces argileuses, par exemple, des polyanions
qui
attirent à leur
surface des charges positives, et peuvent ainsi servir de supports à d'autres
charges négatives ; ce sont donc éventuellement des
intermédiaires
obligés.
Or, parmi ces molécules il y a une classe, celle des ARN de
transfert, qui est justement au cœur du passage du programme
génétique à son
expression, et ces molécules sont très impliquées
dans le métabolisme actuel ; elles sont d'ailleurs fortement
affectées
par de petites modifications semblables à celles qui se déroulent
dans le métabolisme intermédiaire, et on les découvre
aujourd'hui dans un grand nombre de réactions qui n'ont rien à voir
avec la réaction de fabrication des protéines qui est
leur lieu normal de fonctionnement. On peut les trouver, par exemple,
associées à la
fabrication de liens peptidiques (entre acides aminés — le
cœur
de la synthèse des protéines), et l'on peut donc très
bien les imaginer comme étant des ancêtres de cette
réaction,
auquel cas la formation de liens peptidiques à partir de molécules
comme les ARN de transfert aurait été antérieure à l'utilisation
de cette formation de liens peptidiques dans la synthèse des
protéines
comme on la connaît aujourd'hui. Voici donc des objets bien
réels
qui ont pu jouer ce rôle de support métabolique, ce
qu'on peut essayer de mettre en évidence dans un certain nombre
d'organismes. - Schéma : Formation d'une liaison peptidique
entre deux amino-acides adénylates pris "en sandwich" entre
deux feuillets d'argile. -
 Robert
Pascal poursuit ses questionnements. Est-ce que ce métabolisme
s'est organisé selon
l'hypothèse
d'Oparin et Haldane (hétérotrophie)
ou autour d'une source minérale d'énergie (autotrophie)
? L’hétérotrophie est la nécessité pour
un organisme vivant de se nourrir de constituants organiques préexistants.
L’autotrophie désigne la capacité de certains organismes
vivants à produire de la matière organique en procédant à la
réduction de matière inorganique, par exemple le carbone
(le dioxyde de carbone) ou encore l’azote (sous forme de NO3, nitrate,
ou de N2, diazote). Cela s’accompagne d’un prélèvement
de sels minéraux dans le milieu (ions nitrate, phosphate…).
Les organismes autotrophes sont donc capables de se développer
dans un milieu ne contenant que du carbone minéral, contrairement à un
organisme hétérotrophe qui devra se procurer des molécules
organiques (idem pour l’azote). Ce
mode de nutrition caractérise les végétaux chlorophylliens
(verts), les cyanobactéries, les bactéries sulfureuses. L’énergie
nécessaire à cette synthèse provient, soit de la
lumière grâce à la photosynthèse
dans les cellules chlorophylliennes, soit des liaisons chimiques,
grâce à la chimiosynthèse des
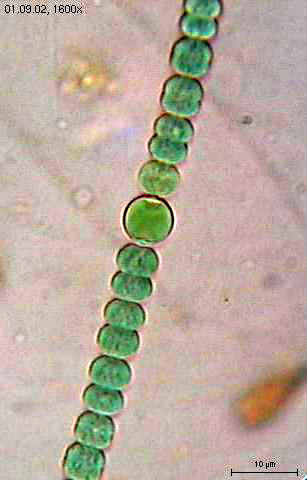
bactéries sulfureuses, par exemple. - Photo :
Algue bleue, Cyanobactérie,
Anabaena sperica. -
Robert
Pascal poursuit ses questionnements. Est-ce que ce métabolisme
s'est organisé selon
l'hypothèse
d'Oparin et Haldane (hétérotrophie)
ou autour d'une source minérale d'énergie (autotrophie)
? L’hétérotrophie est la nécessité pour
un organisme vivant de se nourrir de constituants organiques préexistants.
L’autotrophie désigne la capacité de certains organismes
vivants à produire de la matière organique en procédant à la
réduction de matière inorganique, par exemple le carbone
(le dioxyde de carbone) ou encore l’azote (sous forme de NO3, nitrate,
ou de N2, diazote). Cela s’accompagne d’un prélèvement
de sels minéraux dans le milieu (ions nitrate, phosphate…).
Les organismes autotrophes sont donc capables de se développer
dans un milieu ne contenant que du carbone minéral, contrairement à un
organisme hétérotrophe qui devra se procurer des molécules
organiques (idem pour l’azote). Ce
mode de nutrition caractérise les végétaux chlorophylliens
(verts), les cyanobactéries, les bactéries sulfureuses. L’énergie
nécessaire à cette synthèse provient, soit de la
lumière grâce à la photosynthèse
dans les cellules chlorophylliennes, soit des liaisons chimiques,
grâce à la chimiosynthèse des
bactéries sulfureuses, par exemple. - Photo :
Algue bleue, Cyanobactérie,
Anabaena sperica. -
Partant de l'hypothèse d'une continuité évolutive entre la chimie prébiotique et la chimie biologique, Robert Pascal postule que l'origine de la vie remonte à l'émergence d'un polymère génétique à partir d'un réseau de réactions chimiques (protométabolisme) reposant sur l'activité de petites molécules ou de molécules ne portant pas d'information. Ce protométabolisme a dû constituer une "niche écologique" favorable au développement d'un réplicateur génétique. Il analyse donc la vie comme une propriété émergente (Cf. The Emergence of Life on Earth: A Historical and Scientific Overview by Iris Fry), et suppose qu'une transition a eu lieu à partir d'une chimie prébiotique en évolution. Cette transition s'analyse comme une auto-organisation où l'entropie (le désordre) du système a diminué. A ce stade, la formation des peptides/acides nucléiques a dû se produire au sein d'un métabolisme de ces composés. On ne peut pas distinguer le stade de formation des monomères de celui de leur activation/polymérisation. Toutefois, bien que l'ARN semble incontournable, Robert Pascal est conscient de la très grande difficulté de le synthétiser dans un contexte prébiotique, avec d'abord la formation abiotique de nucléotides, puis leur polymérisation. Selon Hud et son équipe (PNAS 2010), la polymérisation spontanée de l'ARN a nécessité deux processus distincts, celui de la régiosélectivité et celui de la cyclisation des brins. Robert Pascal s'interroge sur le fait de savoir comment un monde d'ARN a pu exister et évoluer sans protéines codées, et si l'ARN a eu un prédécesseur qui n'a pas laissé de trace dans l'évolution.
Il se demande également si cette émergence
s'est faite au cours d'un processus ponctué de plusieurs étapes : Briques
du
vivant, Polymères,
Interactions
supramoléculaires ? Jean-Marie Lehn (Prix Nobel
1987 de Chimie) formalise ce dernier concept.
Au-delà de la chimie moléculaire, fondée
sur la liaison covalente, s'étend un domaine qu'on
peut nommer supramoléculaire.
Des briques moléculaires, une fois mélangées
en solution dans des conditions contrôlées, s'autoassemblent
pour donner des édifices plus complexes. Bien que le nouveau
système puisse acquérir des propriétés
qu'il ne possédait pas avant l'établissement desdites
liaisons non covalentes, chacune des molécules prenant
part à la
nouvelle "supermolécule" ne voit en rien son
intégrité chimique
modifiée. 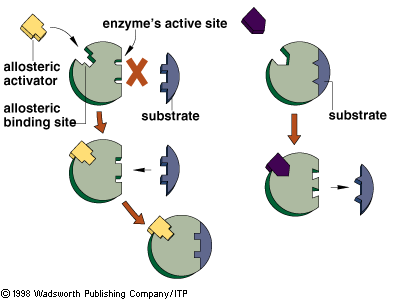 Cependant,
l'architecture de l'assemblage supramoléculaire
peut faire en sorte que certaines molécules soient rendues
plus réactives par perturbation de leur nuage électronique
ou déformation de leurs angles de liaison. Le rapprochement
au sein de l'entité supramoléculaire de deux molécules
naturellement enclines à réagir ensemble peut aussi
les pousser à réagir plus facilement que si elles
avaient été libres dans un solvant. On parle alors
de catalyse supramoléculaire (les enzymes sont l'exemple
le plus connu de catalyseur supramoléculaire biologique). - Schéma :
Enzyme. -
Cependant,
l'architecture de l'assemblage supramoléculaire
peut faire en sorte que certaines molécules soient rendues
plus réactives par perturbation de leur nuage électronique
ou déformation de leurs angles de liaison. Le rapprochement
au sein de l'entité supramoléculaire de deux molécules
naturellement enclines à réagir ensemble peut aussi
les pousser à réagir plus facilement que si elles
avaient été libres dans un solvant. On parle alors
de catalyse supramoléculaire (les enzymes sont l'exemple
le plus connu de catalyseur supramoléculaire biologique). - Schéma :
Enzyme. -
Quelle a été la force motrice de cette émergence ? Il existe diverses positions philosophiques possibles vis-à-vis de la transition du non vivant au vivant, celle de dire qu'il s'agit de la conséquence d'une volonté extérieure, ou alors d'un (ou de plusieurs) événement(s) hautement improbable(s), ou encore d'un (ou de) principe(s) inconnu(s) restant à découvrir et enfin des lois connues de la physique et de la chimie dans un contexte environnemental favorable. L'exobiologie se situe dans ce dernier cas de figure. Robert Pascal cite la position du chimiste israélien Addy Pross qui suggère que la spécificité du vivant soit en fait liée à la stabilité des systèmes capables de se répliquer. Comprise comme la capacité de tels systèmes à occuper l’espace disponible et à se maintenir dans le temps, cette acception n’a que peu de rapports avec la stabilité thermodynamique (*) qui conduit inéluctablement les systèmes chimiques usuels vers l’état d’équilibre. Au contraire, les lois de la cinétique (vitesse des réactions chimiques) conduisent les réplicateurs vers un état de plus grande stabilité cinétique, sélectionnant les variantes les plus à même à se répliquer et tirant parti des modifications de leur propre nature (que l’on appelle les mutations dans un contexte biologique). Une telle description présente l’avantage de proposer qu’une force motrice unique ait gouverné tant l’émergence du vivant que son évolution ultérieure décrite par la théorie darwinienne qui ne devient en quelque sorte qu’une formulation particulière des règles plus générales gouvernant les propriétés des réplicateurs. Ne fournirait-elle pas une base physicochimique à ce que les conceptions vitalistes ont cherché à identifier comme une force vitale spécifique à la matière vivante ?
(*) L'ordre biologique et la thermodynamique. Si l'on considère le vivant comme un système ouvert pouvant échanger à la fois énergie et matière avec le milieu extérieur, celui-ci peut tendre vers un régime constant autre que celui d'équilibre. C'est un état stationnaire de non-équilibre associé à des structures dissipatives qui comportent un principe d'ordre entièrement différent, un "ordre par fluctuation". En ce qui concerne les stades prébiologiques, les travaux d'Eigen montrent que, pour un système formé de protéines et de polynucléotides, les interactions permettraient au système d'atteindre un état final caractérisé par un code génétique et une stabilité remarquable. Le rôle possible des structures dissipatives dans la synthèse abiotique des polypeptides par condensation sur des surfaces catalytiques a été souligné par Katchalsky et al.. Mais le problème le plus fondamental est certainement celui étudié par Eigen concernant l'évolution de populations de molécules d'intérêt biologique et la formation spontanée d'un "code génétique" par une succession d'instabilités qui ont permis de franchir le no man's land entre vie et non-vie.
Pour
qu'il y ait eu émergence,
il a fallu la réunion de plusieurs
facteurs : des voies abiotiques de synthèse
entre des molécules par assemblages, interactions covalentes/non
covalentes jusqu'à obtenir des concentrations suffisantes, par
le biais d'un flux d'énergie assuré par des transporteurs
moléculaires. Les briques du vivant se sont construites avec
les molécules
organiques produites dans le milieu interstellaire, dans l'atmosphère
et autour des sources hydrothermales. Si les acides
aminés (constituants des protéines)
semblent avoir été assez facilement disponibles, il n'en est pas de même
pour les nucléotides
(bases nucléiques,
sucres, phosphorylation) susceptibles de s'assembler pour synthétiser
l'ARN, et il a fallu aussi que se produisent des acides gras. A ce stade,
la synthèse
de l'ARN ne s'est probablement pas faite à partir
des briques utilisées par les biochimistes. Il y a plutôt
eu une synthèse
prébiotique
de nucléosides à partir
de trois éléments
simples et répandus, le cyanamide,
le formaldéhyde et le cyanoacétylène. Robert Pascal
évoque à ce sujet les travaux de Carole Anastasi,
ainsi que l'intérêt de la réaction de formose.
Elle permet d'obtenir à partir
d'une molécule simple, le formaldéhyde, par polymérisation
autocatalytique en milieu basique, un mélange de produits parmi lesquels
on trouve des sucres complexes comme le ribose, qui constitue un pas
important vers la synthèse
de l'ARN.
Dans une expérience simulant les
conditions de la Terre primitive, des pentoses ont été obtenus à partir
d'un mélange
de formaldéhyde, de glycéraldéhyde et de borates
comme la colémanite Ca2B6O115H2O ou la kernite Na2B4O7. L'intérêt
pour la réaction de formose s'est encore accru lorsque les recherches
en astrochimie ont confirmé la présence de formaldéhyde
et de glycolaldéhyde dans le milieu interstellaire.
En 2009, Powner et
Sutherland sont
parvenus à établir
une voie de synthèse des nucléotides à base
pyrimidique, l'acide uridylique et l'acide cytidylique. Les chercheurs
butaient
sur cette voie de synthèse pré-biotique depuis 40 ans
en raison de la difficulté de trouver la bonne façon
de lier le ribose à la base azotée. La clé de
cette voie a été de passer par un précurseur
commun au ribose et la base azotée. Ce précurseur,
le 2-aminooxazol, est obtenu à partir de molécules
organiques élémentaires
: le glycéraldéhyde, le cyanimide, le cyanoacétaldéhyde,
le cyanoacétylène et le phosphate inorganique. Le mélange
réactionnel alimenté par de l'azote gazeux est soumis à un
cycle de chauffage-refroidissement afin de simuler le cycle d'évaporation
d'une mare par le rayonnement solaire et l'alimentation par la pluie.
Après une semaine le 2-aminooxazol s'accumule dans le réacteur.
Le
précurseur se transforme ensuite en ribose et cytosine
liés
ensemble. Le phosphate, qui permet l'isomérisation, est ensuite
ajouté au
milieu réactionnel
en présence d'UV durant trois jours (l'absence d'ozone dans
les conditions pré-biotiques engendrait un bombardement intense
d'UV). L'acide cytidylique se synthétise sous l'effet du rayonnement
UV et quelques nucléotides portant une cytosine se transforment
en acide uridylique. Pour les deux autres nucléotides, l'équipe
de Sutherland travaille sur un précurseur commun aux acides
nucléiques à base purique. On constate ici qu'à partir
de petites molécules,
on obtient de meilleurs résultats qu'à partir de grosses molécules.
- Remarque : Le phosphore,
indispensable à cette réaction, n'est pas observé dans
le milieu interstellaire, mais il y en avait sur Terre. David Bryant et son équipe
s'intéressent à
l'oxydation du phosphore dans les météorites.
- Schémas : ARN, un nombre énorme de
combinaisons possibles. Conversion d'une
forme physique d'énergie en une espèce chimique riche en énergie,
une molécule activée transporteur d'énergie (Boiteau
& Pascal, Orig. Life Evol. Biosph. 2010). -
Le
système
obtenu ne peut pas être
isolé, car il nécessite
une source d'énergie
chimique proportionnée à la
hauteur de la barrière cinétique
déterminant
la vitesse de réaction (Selon
le chimiste Arrhénius,
pour qu'une réaction chimique
puisse se produire, il faut qu'il y ait
une quantité d'énergie
minimale pour «propulser» les
molécules d'un état chimique à un
autre). Par exemple, dans
l'atmosphère, la photolyse, c'est à dire
la dissociation de molécules, ne peut
se produire que si les
photons possèdent une énergie supérieure
ou égale à la liaison covalente, qui
est de 435 kJ/mol pour l'hydrogène gazeux
H2, 532 kJ/mol pour le gaz carbonique
CO2, et 945 kJ/mol pour l'azote gazeux
N2. Les décharges électriques dépassent
la température de 10 000 Kelvin. - Schéma
: Les NCA, des transporteurs d'énergie potentiels (Biron, Parkes,
Pascal, Sutherland, Angew. Chem. Int. Ed. 2005). -
Sachant que
la catalyse et les températures élevées
permettent d'évoluer plus rapidement
vers l'état
d'équilibre,
mais
ne permettent pas d'utiliser l'énergie
chimique, la source d'énergie
chimique se trouve donc dans des réactions
couplées,
constituant une boucle catalytique.
La "pompe
primaire" est
constituée
par le protométabolisme
des acides aminés (Cf. 'L'environnement
de la Terre primitive, p 372, Muriel Gargaud), où les N-carboxyanhydrides
d'acides aminés (NCA) sont des transporteurs d'énergie
potentiels. 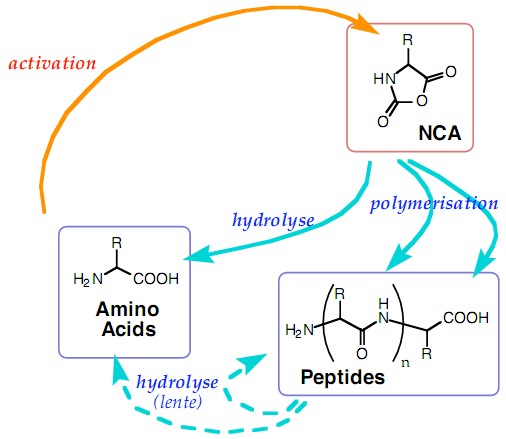 Robert
Pascal montre les formules de synthèse d'acides aminés
et de peptides, ainsi que les caractéristiques des acides
alpha aminés dans la réaction de Strecker, celle de
Bucherer-Bergs effectuée par l'équipe de Taillades,
les acides alpha-aminés
activés obtenus par l'équipe Commeyras qui étudie également
la synthèse préalable des N-carboxyanhydrides d'acides aminés
(NCA) et le système
dynamique acide alpha-aminé-peptide. - Schéma :
Protométabolisme des acides aminés. -
Robert
Pascal montre les formules de synthèse d'acides aminés
et de peptides, ainsi que les caractéristiques des acides
alpha aminés dans la réaction de Strecker, celle de
Bucherer-Bergs effectuée par l'équipe de Taillades,
les acides alpha-aminés
activés obtenus par l'équipe Commeyras qui étudie également
la synthèse préalable des N-carboxyanhydrides d'acides aminés
(NCA) et le système
dynamique acide alpha-aminé-peptide. - Schéma :
Protométabolisme des acides aminés. -
Il
met en évidence le nombre
immense de combinaisons possibles dans ces assemblages. Pour les protéines,
composées d'acides aminés choisis parmi les 20 utilisés dans le vivant,
il y en a 20 à la puissance 100, soit 10 à la puissance 130 ! L'ARN,
lui, comporte 4 bases différentes, ce qui donne 4 à la puissance 100
ou 10
à la puissance 60. Cela fait plus de molécules
possibles que d'atomes dans l'univers... Ce résultat est lié au
fait qu'il s'agit de structures en trois dimensions, dont la diversité
tient au nombre de molécules qu'elles comportent, à l'ordre dans lequel
celles-ci sont agencées (les séquences), à la forme qu'elles prennent
(car elles peuvent se replier sur elles-mêmes),
et enfin à leur orientation (chiralité) 'droite'
ou 'gauche' (comme les deux mains) qui induit des propriétés
différentes.
Parmi ces
deux dernières formes, le vivant n'en utilise qu'une, droite ou gauche
selon la catégorie de molécule. Dans
un système dynamique (hors équilibre), l'état racémique
qui existe à l'origine (c.a.d. comportant un nombre égal de molécules
de formes 'droite' et 'gauche') peut devenir instable
et il se produit alors une amplification autocatalytique
de la chiralité étudiée
par Plasson,
Bersini, Commeyras (PNAS 2004) et Danger, Plasson, Pascal (Astrobiology 2010)
: le système bascule en L (gauche) ou D (droite).
- Les acides aminés L représentent
la quasi totalité des acides aminés qui se trouvent dans les
protéines. Les acides aminés D se rencontrent dans certaines
protéines produites par des organismes exotiques au fond des océans,
comme certains mollusques. Ce sont également des composants abondants
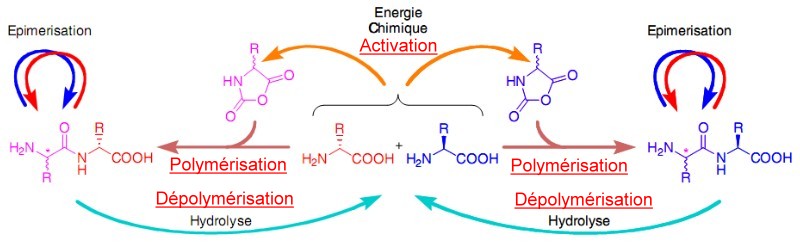
des parois cellulaires des bactéries. - L'émergence
de cette homochiralité,
caractéristique du vivant,
s'effectue selon le processus APED (Activation
/ Polymerisation / Epimerisation
/ Dépolymérisation).
Ce système n'échappe
pas aux lois de la thermodynamique, mais la thermodynamique est
inapte à la description
de son originalité qui est
principalement de nature cinétique. Le
réseau autocatalytique
(réplicateur) se forme avec une compétition
pour
consommer l'énergie, ce qui fournit une "Sélection
naturelle" du PLUS RAPIDE, du plus
efficace à se reproduire. Un polymère, porteur
d'information en interaction chimique, stabilise le réseau
auto-catalytique. Si l'auto-organisation est gouvernée
par un impératif cinétique, chercher à caractériser
la transition par l'étude
des produits stables
est insuffisant.
L'analyse cinétique est nécessaire et il faudra
donc développer
les études de cinétique en solution aqueuse et
rechercher des réactions couplées.
Le processus d'évolution, abiotique ou biotique, se traduit par une sélection. Celle-ci peut s'effectuer à trois niveaux différents : tout d'abord l'organisme, ensuite la fonction ou la propriété (d'une macromolécule) que porte cet organisme, liée à la structure et à la séquence de la macromolécule dont la variabilité permet l'évolution. La sélection se produit enfin par des variations (mutations) au sein de la séquence d'une macromolécule qui offrent une source quasi-infinie de diversité. Reste à comprendre en fonction de quoi celles-ci sont sélectionnées.
Selon
Biron, Parkes, Pascal, Sutherland, un lien entre
les chimies des acides aminés et des nucléotides pourrait être à l’origine
de la machinerie de traduction du code génétique. Pour comprendre
les premiers stades du vivant, il faut imaginer un scénario
d’apparition du mécanisme de traduction reposant non seulement
sur une évolution non-déterministe mais aussi sur une force
motrice ayant conduit à la sélection du système actuel
sophistiqué.
La détermination de la structure tridimensionnelle du ribosome
montrant l’absence de toute protéine à proximité du
site de formation de la liaison peptidique est souvent considérée
comme un argument en faveur d’un rôle initial important pour
les ARN (monde d'ARN)
qui
auraient alors servi simultanément
de supports pour l’information et de catalyseurs indispensables au
fonctionnement d’un système capable d’autoreproduction.
Mais une matrice optimale pour porter l’information requiert une morphologie
uniforme adaptée à une recopie linéaire tandis qu’une
activité catalytique diversifiée nécessite un large éventail
de structures possibles pour s’adapter aux besoins des réactions à catalyser.
La vie n’a pu remplir ces deux exigences contradictoires simultanément
et complètement que par le recours à deux catégories
différentes de polymères, les acides nucléiques et les
protéines, donc après l’apparition du code génétique
et de son mécanisme de traduction. Cette émergence reste obscure
dans un contexte où le moindre avantage sélectif suppose que
plusieurs codons puissent déjà être traduits avec une
fidélité raisonnable en acides aminés, ce qui nécessite
même à ce stade un système très sophistiqué.
- Schémas : Les précurseurs. -
Un
premier pas vient d’être franchi par l’équipe «Dynamique
des Systèmes Biomoléculaires Complexes» (DSBC) en collaboration
avec une équipe
de l’Université de Manchester. Ces travaux
consistent dans la mise en évidence d'un mécanisme chimique
original conduisant à la formation de liaisons covalentes entre acides
aminés
et nucléotides assez semblables à celles que l’on trouve
aujourd’hui entre un acide aminé et l’ARNt. Cette possibilité repose
sur la réactivité des N-carboxyanhydrides d’acides aminés
(NCA) avec un groupement phosphate suivi par une réaction intramoléculaire
très efficace. Des molécules, analogues simplifiés des
aminoacyl-ARNt, peuvent ainsi être obtenues spontanément (sans
nécessiter de
catalyse) par interaction des NCA avec des nucléosides phosphorylés
en positions 3’. Cette réaction pourrait avoir conduit simplement à des
conjugués acides aminés-ARN ouvrant une possibilité d’évolution
ultérieure vers les aminoacyl ARN de transfert. Cette réaction
consolide l’hypothèse d’un rôle important à l’origine
de la vie pour les NCA dont une voie de synthèse compatible avec les
conditions de la Terre primitive a été proposée, il
y a quelques années par l’équipe DSBC. D’autres
arguments en faveur d’un rôle important des NCA aux premiers
stades du vivant viennent également d’être avancés
dans une revue récente sur la chimie prébiotique des acides
aminés et des peptides (Pascal, Boiteau, Commeyras, 2005). Leur grande
réactivité est associée à un contenu énergétique
facilement transférable permettant de les considérer comme
des transporteurs d’énergie. - Schéma
: Les précurseurs. -
On
constate la conversion
d'une forme physique d'énergie en
une espèce chimique
riche en énergie, un transporteur d'énergie. Cette espèce
est caractérisée par sa capacité à donner de
l'énergie
(pouvant être transformée en produit en libérant de l'énergie
libre) et elle est préservée d'une dégradation spontanée
par une barrière cinétique (liaison covalente). L'énergie
peut aussi bien émaner d'une source thermale que de l'activation photochimique
dans l'atmosphère. Elle induit la formation de composés organiques
de faible poids moléculaire qui tendent à s'auto-organiser
grâce à leur capacité à
délivrer des quanta d'énergie correspondant aux premières
réactions biochimiques
et à la reproduction d'entités aptes à leur propre réplication.
Le
mode d'activation dans l'atmosphère s'effectue par la photolyse
(avec des photons d'énergie
supérieure ou égale à celle d'une liaison covalente).
Avec les précurseurs contenus dans la matière
organique extraterrestre, les NCA peuvent produire beaucoup de nucléotides
activés. On constate ainsi une continuité entre les petites
molécules formées dans l'univers ou les atmosphères
planétaires (comme celle de Titan par exemple), et les macro-molécules
qui conduisent au vivant. -
Tableau : Décharges électriques
avec
.
-
| SOMMAIRE | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | Page suivante
|